Endocrinologie
Publié le 05 nov 2013Lecture 14 min
Les perturbateurs endocriniens environnementaux : de nouveaux obésogènes, de nouveaux diabétogènes ?
P. FENICHEL Service d’endocrinologie, diabétologie et reproduction – Inserm U1065, Hôpital de l’Archet 2 – CHU Nice
L’obésité, définie par un indice de masse corporelle (IMC) > 30 kg/m2, est considérée aujourd’hui comme un problème de santé publique préoccupant aussi bien par la gravité de ses conséquences que par sa prévalence en constante augmentation. Cette prévalence a augmenté de façon telle au cours des trois dernières décennies – aussi bien dans les pays industrialisés riches, comme les États-Unis où, en 2008, 60 % des adultes étaient considérés au moins en surpoids (IMC > 26), que dans des pays moins industrialisés, comme la Chine, le Moyen-Orient ou l’Australie, voire dans les pays en voie de développement, plus pauvres, où l’obésité malgré tout peut cœxister avec la sous-nutrition – que l’on parle, à son sujet, d’une véritable épidémie galopante. Les facteurs classiques de suralimentation et de sédentarité survenant sur un terrain génétique prédisposant, considérés à juste titre comme prépondérants, ne permettaient plus à eux seuls d’expliquer les données épidémiologiques, d’où la recherche de facteurs environnementaux.
En outre, l’obésité touche de plus en plus l’adolescent, voire l’enfant, et entraîne, de façon concomitante et parallèle, l’apparition de plus en plus précoce d’un syndrome métabolique avec insulinorésistance ouvrant la voie à la survenue d’un diabète sucré de type 2 (DT2). La prévalence du syndrome métabolique est en nette augmentation à travers le monde, touchant 5 % des adolescents américains tout-venant et 30 % des adolescents obèses. Selon un rapport de 2009, 40 % des Américains âgés de plus de 20 ans étaient considérés comme présentant un diabète ou un prédiabète.
Intrication des facteurs génétiques, comportementaux et environnementaux
Bien que l’étiologie exacte de l’obésité commune, du syndrome métabolique et du DT2 reste méconnue, il est vraisemblable qu’il s’agisse d’une interaction complexe de facteurs génétiques et comportementaux.
Cependant, l’importance et la rapidité de la progression de leur prévalence ainsi que leur extension géographique à travers le globe ont conduit les médecins et les chercheurs à considérer que les facteurs classiques de suralimentation et de sédentarité survenant sur un terrain génétique prédisposant, considérés à juste titre comme prépondérants et justifiant les mesures thérapeutiques entreprises, ne permettaient plus à eux seuls d’expliquer les données épidémiologiques.
C’est la raison pour laquelle les facteurs environnementaux sont aujourd’hui examinés avec de plus en plus d’attention. D’autant que depuis les travaux de David Barker dans les années 1980, l’on sait que des conditions environnementales délétères (stress, carence nutritionnelle ou déséquilibre métabolique), dans certaines périodes critiques du développement comme la période fœtale ou périnatale, tout en s’exprimant dans un premier temps sous la forme d’une hypotrophie fœtale (ou retard de croissance intrautérin), sont capables de programmer à distance la survenue à l’âge adulte d’une obésité, d’un syndrome métabolique et/ou d’un diabète de type 2.
Chez le rongeur sans fond génétique de susceptibilité au diabète, on sait aujourd’hui induire un diabète transmissible sur plusieurs générations en manipulant simplement l’équilibre glycémique de la mère pendant la gestation et donc l’environnement métabolique fœtal.
Une autre condition intra-utérine délétère susceptible de s’exprimer bien des années après la période fœtale et pouvant contribuer à expliquer l’augmentation de l’obésité et du diabète concerne l’exposition maternelle à des polluants organiques persistants exerçant une activité de perturbateur endocrinien environnemental (PEE) et capables de traverser le placenta.
L’hypothèse du rôle de ces composés chimiques en tant qu’obésogène et/ou diabétogène s’appuie à la fois sur :
- l’augmentation croissante de l’utilisation et de la présence de ces produits chimiques dans l’environnement quotidien, tout particulièrement dans la chaîne alimentaire, laquelle suit en parallèle les courbes de prévalence de l’obésité et du diabète ;
- le caractère le plus souvent lipophile de ces produits organiques et leur bioaccumulation dans le tissu graisseux des organismes vivants ;
- les données épidémiologiques humaines et expérimentales in vivo (rongeurs) ou in vitro (culture d’adipocytes ou de cellules pancréatiques endocrines humaines).
Qu’est-ce que les PEE ?
Les PEE sont définis comme des produits chimiques naturels ou de synthèse mimant ou interférant avec la production, l’activité ou le métabolisme des hormones du système endocrine, et susceptibles de perturber la physiologie et de favoriser la survenue de pathologies chroniques du développement ou de la reproduction, de cancers hormonodépendants ou de pathologies métaboliques (obésité, syndrome métabolique, diabète).
Ils sont présents dans l’environnement quotidien, l’air, l’eau, les objets usuels, la chaîne alimentaire en tant que contenants, cosmétiques, surfactants, conservateurs, retardateurs de flamme, etc. Utilisés dans l’agriculture (pesticides organochlorés), dans l’industrie des plastiques (phtalates, bisphényls polychlorés, bisphénol A), ou issus des déchets industriels comme la dioxine, ces substances agissent, par l’intermédiaire de différents récepteurs hormonaux, aux estrogènes, aux androgènes, aux hormones thyroïdiennes, ou à d’autres récepteurs nucléaires comme PPARg impliqués dans le métabolisme des lipides et l’adipogenèse, ou membranaires comme les récepteurs à protéines G.
Ces produits sont théoriquement métabolisés par le foie avec détoxification impliquant leur oxydation par des enzymes de détoxification, les cytochromes P450, puis glucurono ou sulfoconjugués, permettant leur élimination rénale ou entérale. Mais du fait de l’exposition permanente et prolongée, des capacités limitées de détoxification hépatique, et de leur caractère le plus souvent lipophile, ces produits vont également se bioaccumuler dans le tissu graisseux.
Cette bioaccumulation progressive, parfaitement corrélée à l’âge – donc à la période d’exposition –, explique les concentrations élevées retrouvées dans les organismes vivants, malgré une exposition quotidienne à des doses apparemment faibles dans l’environnement.
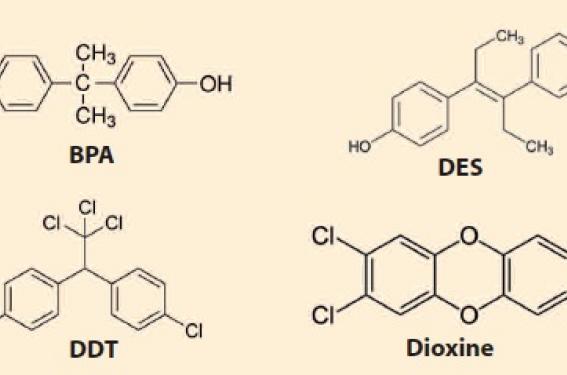
Le cas du BPA et des produits organiques persistants organochlorés comme la dioxine pris ici en exemple permet d’illustrer parfaitement ces concepts émergeants et ces interrogations dans la mesure où, parmi les effets plausibles de ces perturbateurs endocriniens environnementaux (PEE), ont été rapportés des liens avec le diabète et l’obésité, la reproduction et les cancers hormonodépendants, tel que l’a souligné, en particulier pour les maladies métaboliques, le dernier rapport de l’ANSES sur le bisphénol A publié en décembre 2011 (figure 1).
Figure 1. Exemple de 4 perturbateurs endocriniens environnementaux xénœstrogéniques présentant une apparentée structurale sur le plan chimique.
BPA et obésité
Produit chimique synthétisé au début du XXe siècle à partir de 2 molécules de phénol (bisphénol) et une molécule d’acétone (bisphénol A), le BPA a d’abord contribué à la recherche d’un estrogène de synthèse, en raison d’un effet estrogénique mis en évidence sur l’utérus de rongeur. Mais il a été rapidement supplanté par le diéthylstilbestrol (Distilbène®), présentant une forte analogie structurale et un pouvoir estrogénique bien plus puissant.
Le BPA s’est avéré très performant dans la production de plastiques polycarbonés et de résines époxy en raison des propriétés de souplesse et de résistance à la chaleur qu’il introduisait, et son utilisation s’est rapidement étendue à travers le monde à partir des années 1960. Il est retrouvé aujourd’hui de façon extrêmement ubiquitaire dans l’environnement quotidien domestique ou industriel : sacs en plastique, biberons, bouteilles d’eau minérale, canettes de boissons et boîtes de conserve protégées par un fin film plastique interne, prothèses dentaires mais aussi ustensiles ménagers, revêtements automobiles intérieurs, vernis, peintures, CD-Rom, etc. Sa production et sa consommation annuelles sont considérables, estimées à plusieurs millions de tonnes (figure 2). En fait, sa polymérisation incomplète favorise son relargage, accentué par l’élévation de la température ou les modifications de pH, comme par exemple à partir des contenants ou des films plastiques utilisés dans les micro-ondes. Il est retrouvé dans 90 % des urines de la population américaine de référence, à des concentrations comprises entre 0,2 et 1,6 ng/ml (0,88- 7,0 nm) ainsi que dans le sang, le lait maternel ou le liquide amniotique.
Figure 2. La présence de bisphénol A est ubiquitaire dans l’environnement.
Chez la souris, l’exposition prénatale ou néonatale à de faibles doses de BPA, compatibles avec celles retrouvées dans l’environnement domestique, entraîne une augmentation du poids des animaux adultes, variable selon le sexe, la dose et la fenêtre d’exposition, et un syndrome métabolique.
Sur des fibroblastes murins, l’exposition au BPA stimule in vitro la différenciation adipocytaire et l’accumulation lipidique de manière dose-dépendante. De la même manière, sur des adipocytes humains, le BPA à faibles doses inhibe la sécrétion d’adiponectine et stimule la sécrétion d’interleukine-6 et de TNFa, deux adipokines inflammatoires, ce qui suggère son implication possible dans l’obésité, le syndrome métabolique et l’insulinorésistance, avec un effet délétère à la fois sur la balance énergétique et l’homéostasie glucidique (foie, tissu adipeux, îlots pancréatiques).
Dans l’espèce humaine, bien qu’il soit théoriquement rapidement éliminé par voie rénale après glucuronoconjugaison hépatique, le BPA semble néanmoins s’accumuler dans le tissu graisseux, expliquant que son taux sanguin persiste même au cours du jeûne. Sur le plan épidémiologique, une étude française récente a retrouvé une corrélation positive entre les taux de bisphénol urinaire chez la mère et le poids du nouveau-né, proche de ce qui a été décrit chez les rongeurs. Concernant les études épidémiologiques chez l’adulte cherchant à corréler le taux urinaire de BPA et l’obésité, une étude américaine portant sur 2 700 adultes et une étude chinoise parue en 2012 et portant sur 3 400 adultes d’âge moyen corrèlent l’obésité générale, l’obésité centrale et l’insulinorésistance avec les taux urinaires de BPA.
Toutefois, le caractère transversal rétrospectif de ces études – le prélèvement unique de BPA urinaire signant surtout l’exposition récente – interroge sur la liaison causale. Avec honnêteté, les auteurs s’interrogent sur le rôle de la consommation excessive de boissons sucrées, en particulier chez l’obèse, et le relargage de BPA par les cannettes de soda qui sont tapissées d’un mince film plastique. Chez la femme, le taux sanguin de BPA libre est significativement plus élevé en cas de syndrome des ovaires polykystiques (SOPK), endocrinopathie gynécologique très fréquente, associant obésité et insulinorésistance avec laquelle il est corrélé. Aussi, l’exposition au BPA doit-elle être considérée aujourd’hui comme un facteur de risque d’exacerbation et d’accélération dans le développement de l’obésité et du syndrome métabolique.
BPA et diabète
L’utilisation de modèles animaux, de cellules b-pancréatiques murines ou humaines in vitro et plusieurs études épidémiologiques suggèrent que l’exposition au BPA pourrait également participer à l’augmentation de l’incidence du diabète de type 2. L’exposition au BPA de souris mâles adultes provoque un hyperinsulinisme et une insulinorésistance modérée. Il s’agit d’un effet direct sur le pancréas, mais également d’une perturbation de la signalisation insulinique au niveau des tissus périphériques (muscle, foie et tissu adipeux). Le BPA induit dans le foie de rongeur un stress oxydatif en diminuant l’expression des enzymes antioxydantes.
Au niveau de l’adipocyte, il a été montré que le BPA augmente le transport du glucose basal et qu’il est stimulé par l’insuline via une augmentation de l’expression du transporteur GLUT4. Au niveau du pancréas endocrine, le BPA est capable de supprimer, in vitro sur des cellules a-pancréatiques murines, les oscillations calciques induites par le glucose et contrôlant la sécrétion de glucagon. Sur les cellules b, le BPA, à des doses très faibles (0,1 nM), augmente la fréquence des oscillations calciques induites par le glucose stimulant la sécrétion insulinique. Ces effets rapides ont été retrouvés in vitro sur des îlots pancréatiques murins. Ces effets membranaires miment l’action des estrogènes et passent par des récepteurs membranaires non classiques des estrogènes. In vivo, le BPA, de façon rapide (30 min), est capable, comme l’estradiol, d’abaisser la glycémie en provoquant une hypersécrétion d’insuline et de stimuler le facteur de transcription AMP-dépendant CREB, qui régule l’expression du gène de l’insuline et la survie des cellules b. Si l’on prolonge l’exposition au BPA chez le rat, apparaît, au bout de 4 j, un hyperinsulinisme traduisant une insulinorésistance objectivée par les tests d’insulinosensibilité.
Est-il possible d’extrapoler à l’espèce humaine ?
Deux types d’arguments récents vont dans ce sens :
- la répétition des effets rapides in vitro du BPA constatés de la même façon sur des îlots b-pancréatiques humains ;
- plusieurs études épidémiologiques transversales rétrospectives.
Ces études transversales rétrospectives proviennent toutes des enquêtes américaines de la National Health and Nutrition Examination Survey (NHANES). La première, portant sur des adultes représentatifs de la population générale âgés de 18 à 74 ans inclus durant la période 2003- 2004, retrouve, après normalisation pour l’âge, le sexe, l’ethnie, le niveau d’éducation, le tabagisme, l’IMC, le tour de taille et le taux de créatinine urinaire, une corrélation entre la concentration urinaire de BPA et l’existence d’un diabète auto-déclaré. Une corrélation positive a été également retrouvée avec les maladies cardiovasculaires. Le fait que les taux les plus élevés de BPA soient retrouvés pour les valeurs hautes d’IMC et qu’ils ne représentent théoriquement que l’exposition très récente, en particulier à la suite de la consommation de soda (canettes, bouteilles plastiques), très prisée chez les obèses, conduit ici aussi les auteurs à s’interroger sur le lien causal par rapport au rôle d’une exposition prolongée à faibles doses, tout en reconnaissant que cette liaison pourrait indirectement constituer un indicateur d’exposition à de multiples perturbateurs endocriniens. Plusieurs enquêtes similaires menées de 2005 à 2008 retrouvent des résultats discordants. Néanmoins, reprenant des patients des trois enquêtes pour lesquels des résultats biologiques étaient disponibles, Shankar et al. retrouvent une corrélation positive, après correction de tous les facteurs confondants sus-cités, avec le diabète défini soit par une glycémie à jeun > 1,26 g/l ou non à jeun > 2,00 g/l, soit par un taux d’HbA1c > 6,5 %. Ce facteur de risque, indépendant des facteurs traditionnels de risque de diabète de type 2, doit être confirmé par des études prospectives longitudinales.
POP organochlorés
Les POP organochlorés sont les plus anciens, les plus abondants, les plus lipophiles et les moins biodégradables des polluants chimiques persistants à activité de perturbateur endocrinien (figure 3). Ils comprennent les bisphényls polychlorés ou PCB, utilisés dans l’industrie (transformateurs électriques), les pesticides organochlorés utilisés dans l’agriculture et les dioxines libérées par les déchets industriels incinérés. Ils ont été introduits dans les années 1940, utilisés de façon intensive pendant plusieurs décennies puis interdits progressivement dans les pays industriels avancés en raison de leur persistance dans l’environnement et de leur toxicité. Néanmoins, ils restent largement utilisés dans les pays en voie de développement, tel le DDT en Asie, et sont retrouvés en fait dans les pays où ils ont été bannis, dans les nappes phréatiques (longue demi-vie comme le DDE dérivé du DDT [> 50 ans], ou la chlordécone, un pesticide utilisé aux Antilles jusqu’à il y a quelques années, ou l’atrazine en Bretagne) ou dans les graisses animales où ils se sont bioaccumulés en raison de leur résistance à la biodégradation (PCB et poissons du Rhône interdits à la consommation) et de leur caractère très lipophile. Ils sont généralement encore retrouvés dans la plupart des études épidémiologiques humaines.
Figure 3. Mode d’action de différents produits organiques persistants (POP) à activité de perturbateurs endocriniens environnementale dans le cadre de leur effet potentiellement obésogène et diabétogène (d’après P. Grandjean, 2011).
Les bisphényls polychlorés (PCB)
Les PCB sont des produits chimiques résistants aux hautes températures, isolants électriques, très lipophiles, théoriquement interdits mais retrouvés encore dans la majorité des études humaines. In vitro, ils peuvent stimuler la différenciation adipocytaire, la sécrétion d’adipokines inflammatoires et promouvoir l’expression de PPARg. Chez la femme obèse, le taux de PCB-153 a été corrélé négativement avec l’adiponectine, ce qui va dans le sens d’une insulinorésistance. Mais les données concernant leur rôle dans l’obésité et le syndrome métabolique sont parfois contradictoires.
Les pesticides organochlorés
Ils ont été ou sont toujours utilisés dans l’agriculture et sont nombreux.
Le DDE persistant, dérivé du DDT, encore généralement retrouvé dans les prélèvements humains, est concerné en raison de certaines données épidémiologiques retrouvant une corrélation entre l’exposition maternelle, la prise de poids accélérée dans les 6 premiers mois et la survenue de l’obésité de l’adolescence.
D’autres pesticides organochlorés sont soit encore utilisés, soit également présents dans les nappes phréatiques. Dans un travail coréen et norvégien de 2010 étudiant les corrélations entre les taux circulants à l’âge adulte de 22 pesticides organochlorés et le syndrome métabolique, une relation significative a été retrouvée pour trois d’entre eux, l’heptachlore époxyde, le trans-nonachlor et le bêta-hexachlorohexane (bHCH) d’autant que pour ce dernier, une corrélation positive avec l’IMC et l’insulinorésistance a été confirmée dans une autre étude belge récente. Des études in vitro sur l’adipocyte et épidémiologique sur le risque de diabète de type 2 impliquent également le chlordane et l’hexachlorobenzène (HCB).
Les dioxines
Les dioxines sont des composés polyaromatiques oxygénés et polyhalogénés, produits au cours de la combustion dans les incinérateurs d’ordures ménagères, certaines usines chimiques et l’industrie du papier. Le plus connu, la dioxine de Seveso ou TCDD (2, 3, 7, 8-tétrachlorodibenzo- p-dioxine), est un perturbateur endocrinien et métabolique avec des effets anti-adipogenèse, pro-inflammatoire et anti-insuline, médiés par un récepteur intracellulaire particulier, AhR ou aryl hydrocarbon receptor. Lors d’expositions à fortes doses comme l’accident de l’usine de Seveso en Italie ou l’utilisation par les Américains lors de la guerre du Vietnam d’un défoliant à forte concentration de dioxine, l’agent orange, il a été possible de corréler les taux sanguins de dioxine aux troubles métaboliques et au diabète avéré. Dans les études nutritionnelles de populations faiblement exposées aux États-Unis, une relation dose-réponse entre le taux sanguin de dioxine et l’incidence du diabète de type 2 a été mise en évidence. Chez le rongeur exposé, il apparaît rapidement une perte de poids avec hypophagie, et une hyperlipidémie liée à une réduction de captage du glucose par les adipocytes, le foie et le pancréas par anomalie d’expression de son transporteur GLUT 4. Par ailleurs, une dysfonction des cellules b-pancréatiques s’accompagne de troubles de la sécrétion d’insuline.
Conclusion
Bien que leur participation dans la physiopathologie de l’obésité et du diabète ne soit pas formellement démontrée, il existe des présomptions sérieuses sur le rôle éventuel du bisphénol A, présent de façon ubiquitaire dans l’environnement quotidien, qui pourrait, à faibles doses significatives dans l’environnement, dans des périodes critiques d’exposition en particulier (fœtale et/ou périnatale), favoriser le développement de maladies métaboliques, de troubles de la reproduction ou de cancers hormonodépendants (prostate, côlon, testicule) chez des sujets présentant une susceptibilité génétique.
Des études épidémiologiques longitudinales prospectives sont nécessaires pour confirmer une telle responsabilité ainsi que la caractérisation de biomarqueurs capables d’évaluer la durée et l’intensité de l’exposition et de reconnaître les empreintes moléculaires induites par celle-ci (hyperméthylation de gènes, microARN).
Mais l’évaluation du rôle de cette exposition sur la santé humaine, hormis le cas exceptionnel et malheureux du Distilbène®, s’avère en fait très difficile à démontrer sur le plan méthodologique, concernant les aspects toxicologique, épidémiologique ou mécanistique. Elle constitue pourtant un défi aussi bien pour les médecins et les scientifiques chargés d’apporter les preuves de la toxicité ou de l’innocuité d’une molécule que pour les politiques chargés de définir les normes des seuils d’exposition tolérables et d’établir les autorisations et/ou les interdictions de mise sur le marché de nouveaux produits chimiques (programme REACH).
Le débat actuel, qui consiste à savoir s’il faut s’appuyer sur ces éléments de présomption et sur le principe de précaution afin de modifier la réglementation, française ou européenne, et procéder sans tarder à certaines interdictions, par exemple les biberons en plastique, plutôt que de considérer qu’il est « urgent d’attendre » des études à venir – pharmacocinétiques, expérimentales et épidémiologiques –, est par conséquent légitime.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :