Thérapeutique
Publié le 30 nov 2014Lecture 15 min
Sulfamides hypoglycémiants : 70 ans de hauts et de bas ! Où en sommes-nous ?
L. MONNIER, C. COLETTE, Institut universitaire de recherche clinique, Montpellier
Comme tous les médicaments, les sulfonylurées sont passées par différentes périodes au cours de leur longue histoire qui a débuté il y a plus de 70 ans(1).
En général, l’apparition d’un nouveau médicament provoque toujours un enthousiasme initial avec une flambée de prescriptions, qui retombe souvent au bout de quelques mois quand les résultats escomptés ne sont pas totalement au rendez-vous, quand les premiers effets secondaires néfastes apparaissent ou quand une nouvelle classe thérapeutique vient le concurrencer. Ainsi, à la phase d’enthousiasme succède une phase de stabilisation. L’évolution ultérieure dépend de nombreux facteurs. Les effets indésirables réels ou allégués par certaines études peuvent être jugés suffisamment sévères pour « condamner » le médicament.
Ce fut le cas pour la rosiglitazone, condamnée par la métaanalyse de Nissen(2). Depuis elle a été partiellement réhabilitée. Malgré cela, ce médicament est poursuivi, à tort ou à raison, par une mauvaise réputation qui a entraîné son retrait dans la majorité des pays et conduit à une prescription plus que confidentielle dans quelques états des États-Unis. Dans certains cas, après une période de déception et de doute, le médicament retrouve une nouvelle jeunesse et peut même devenir un médicament jugé comme très important. Cette histoire fut celle de la metformine, qui après une phase de rejet en particulier sur le continent américain, est devenue un médicament clé dans le traitement du diabète de type 2, dès lors que les Américains découvrirent ou redécouvrirent en 1995 ses propriétés bénéfiques, alors que ce produit était commercialisé en Europe depuis 1957, malgré un chemin un peu chaotique semé de doutes et de réhabilitations.
Qu’en est-il des sulfonylurées ? Leur histoire s’apparente-t-elle au modèle général que nous venons d’évoquer et quelle place peut-on leur attribuer aujourd’hui au sein d’un arsenal thérapeutique qui ne cesse d’évoluer ?
Le début de l’histoire
L’histoire commence au matin du 27 mars 1942 dans le service des maladies infectieuses, dirigé par le professeur Marcel Janbon, à l’hôpital Saint-Éloi de Montpellier. Chez un garçon de 15 ans, atteint de fièvre typhoïde, traité depuis 3 jours par un sulfamide en essai clinique (le 2254 RP), l’attention du corps médical est attirée par une chute thermique brutale, une légère agitation, quelques troubles visuels et une difficulté à la mobilisation active des muscles. Dans un premier temps, les troubles observés sont interprétés comme une conséquence de la chute thermique. La dose de sulfamide est réduite de moitié et une injection de sérum glucosé est pratiquée en l’absence de toute information biologique. Une amélioration est rapidement observée. Devant la constatation d’un taux plasmatique de sulfamide anormalement élevé, le traitement par le 2254 RP est arrêté. Néanmoins, le sujet entre 3 heures plus tard dans un coma profond, qui cède avec une perfusion intraveineuse de sérum glucosé hypertonique. La récupération finit par être définitive.
Compte tenu de l’histoire clinique, M. Janbon et les membres de son équipe pensent que les accidents présentés étaient dus à des hypoglycémies bien que la glycémie, perturbée par des périodes de resucrages successifs, n’ait jamais été observée à un taux inférieur à 0,70 g/l. Alertés par cette observation, M. Janbon et coll. furent amenés à réaliser une analyse rétrospective de 10 cas de patients traités depuis le mois d’août 1941 par le 2254 RP. Pour asseoir la présomption de culpabilité du 2254 RP dans les accidents présentés par les malades, M. Janbon et coll. administrèrent ce médicament à des sujets sains chez lesquels ils observèrent une baisse de la glycémie allant de 0,20 à 0,50 g/l. Ayant désormais la conviction que le 2254 RP provoquait des hypoglycémies et estimant que l’étude du mécanisme de ces hypoglycémies dépassait ses compétences de clinicien, M. Janbon fit appel avec beaucoup d’honnêteté et de clairvoyance à ses collègues physiologistes de la Faculté de médecine de Montpellier.
Auguste Loubatières, qui était alors chef de travaux dans le laboratoire de physiologie, fut enthousiasmé par la proposition. Il se mit immédiatement à l’ouvrage et dès le mois de juin 1942, il obtint les premiers résultats avec l’observation d’une chute progressive, marquée et durable, de la glycémie chez le chien après administration de 2254 RP. En comparant les courbes obtenues avec celles qu’il avait précédemment observées avec l’insuline IPZ, A. Loubatières eut la géniale intuition que le 2254 RP agissait probablement en stimulant la sécrétion insulinique pancréatique. Cette hypothèse fut rapidement confirmée par la constatation que le 2254 RP n’entraînait pas d’hypoglycémie chez le chien pancréatectomisé. La démonstration définitive fut apportée en 1946 grâce à une expérience de circulation croisée qui consista à anastomoser la veine pancréatico-duodénale d’un chien normal donneur à la veine jugulaire d’un chien receveur rendu diabétique par l’alloxane. L’injection de sulfamide au donneur fut suivie d’une diminution de l’hyperglycémie chez le receveur. Ainsi, dès la fin des années 40, A. Loubatières démontra que le 2254 RP, précurseur des futurs sulfamides hypoglycémiants, était un insulinosécrétagogue, qui ne pouvait agir qu’en présence d’une sécrétion résiduelle d’insuline au niveau du pancréas. Pendant plusieurs années, la communauté scientifique française sous-estima l’importance des travaux d’A. Loubatières. Cette indifférence cessa lorsque Bernardo Houssay, prix Nobel de Médecine, puis Charles Best, codécouvreur de l’insuline, confirmèrent dans les années 50 la validité des travaux d’A. Loubatières.
L’histoire des sulfonylurées prend de l’importance
L’ampleur de cette découverte fut ultérieurement mise en exergue par les auteurs allemands qui publièrent en 1955 les résultats qu’ils avaient obtenus avec le carbutamide (sulfamide voisin du 2254 RP) dans un journal allemand, Deutsche Medizinisch Wochenschrift. Dans leur bibliographie, ils mentionnaient les travaux de Loubatières, reconnaissant ainsi l’antériorité et le caractère pionnier de ses travaux. Toutefois, le véritable départ des sulfamides hypoglycémiants se situa en 1956, lorsqu’un groupe de chercheurs allemands, parmi lesquels A. Bauder et G. Slöter publièrent les résultats expérimentaux et cliniques qu’ils avaient observés avec un troisième sulfamide, le tolbutamide. Ce produit, dépourvu de toute activité bactériostatique ne gardait que les propriétés hypoglycémiantes de ses prédécesseurs, le 2254 RP et le carbutamide. Dès lors, tout était prêt pour que le carbutamide et le tolbutamide soient utilisés dans le traitement du diabète sucré de type 2. C’est ce qui se produisit au cours de l’année 1956 avec la mise sur le marché, en France, des deux produits. Le tolbutamide (Dolipol®), étiqueté sulfamide de 1re génération en raison de son efficacité modeste, même lorsqu’il était prescrit à des doses relativement élevées (500-1 500 mg/jour), a poursuivi sa carrière pendant de nombreuses années avant d’être remplacé.
La suite fut marquée par l’apparition du chlorpropamide (Diabinèse®), sulfamide de 1re génération, mais qui était deux fois moins dosé que le tolbutamide (250 à 750 mg/j). Toutefois, la grande avancée en matière de sulfonylurées fut la mise sur le marché, dans les années 1970, des sulfamides de 2e génération dits « microdosés » : glibenclamide (Daonil®), glipizide (Glibenèse®, Minidiab®) et gliclazide (Diamicron®). Plus tard, fut commercialisé le glimépiride (Amarel®). En dépit de différences que nous développerons plus loin, les sulfamides de 2e génération ont pour caractéristique d’être plus actifs que les sulfamides de 1re génération et surtout de pouvoir être utilisés à des doses de quelques milligrammes (5 à 15 mg/j pour le glibenclamide, le glipizide et le glimépiride) ou de quelques dizaines de milligrammes (30 à 120 mg/j pour le gliclazide LM) alors que les sulfamides de 1re génération ne devenaient efficaces qu’à une posologie quotidienne de quelques centaines de milligrammes. À titre d’exemple, le chlorpropamide, le glipizide et le glibenclamide furent utilisés dans le bras sulfonylurée de l’UKPDS(3), le chlorpropamide ayant été prescrit à une dose allant de 100 à 500 mg/j, tandis que les posologies du glibenclamide et du glipizide étaient comprises respectivement entre 2,5 et 20 mg/j et entre 2,5 et 40 mg/j.
Deuxième partie du XXe siècle : l’âge d’or des sulfonylurées
L’enthousiasme pour les sulfonylurées, qui marqua une bonne moitié de la deuxième partie du XXe siècle fut grevé de quelques déceptions. Toutefois, pendant de nombreuses années, de 1956 jusqu’aux années 90 (date de la commercialisation des alpha-glucosidases), les sulfonylurées restèrent avec les biguanides (metformine essentiellement) les deux « vedettes » indiscutables de la thérapeutique orale du diabète de type 2, désigné à ce moment-là comme diabète de la maturité ou non insulinodépendant(4). En effet, dans les années 1970, l’insulinothérapie apparaissait comme une mesure thérapeutique relativement exceptionnelle dans le diabète de type 2, réservée à quelques cas particuliers. Depuis heureusement, les stratégies thérapeutiques ont bien changé puisque l’insulinothérapie s’est banalisée dans le diabète de type 2, avec tous les ans, en France, un passage au traitement insulinique chez 80 000 diabétiques de type 2.
À partir de ce constat, en faisant un retour en arrière sur les années 70-80, on s’aperçoit que les organigrammes thérapeutiques de l’époque étaient relativement simples. Le traitement de première ligne dépendait du poids du sujet : metformine s’il était excessif et sulfonylurée s’il était normal ou subnormal(4). Les sujets obèses étaient considérés surtout comme insulinorésistants et les sujets de poids normal ou maigres, comme insulinoprives. Dans ces conditions il n’était pas illogique de proposer aux premiers un insulino-sensibilisateur (la metformine) et aux seconds un insulino-sécrétagogue (une sulfonylurée). Quand la monothérapie s’avérait insuffisante, il était habituel de proposer une bithérapie associant biguanide et sulfonylurée(4). Ainsi, ces deux classes thérapeutiques se partageaient la prescription pharmacologique du diabète de type 2, y compris en première intention alors qu’aujourd’hui, pour de multiples raisons, les plus importantes étant d’ordre physiopathologique, toutes les organisations reconnaissent que la metformine est le premier traitement à instaurer dans le diabète de type 2 au moment de la découverte de la maladie(5).
Cet enthousiasme pour les sulfonylurées fut toutefois tempéré par la publication en 1970 des résultats de l’UGDP (University Group Diabetes Program)(6). Cette étude avait été conçue pour suivre 5 groupes de patients (200 dans chaque groupe) ayant un diabète de la « maturité » (qualificatif utilisé à l’époque pour désigner le diabète de type 2) et classés en fonction du type de traitement auquel ils avaient été affectés. Après 8 ans et demi de suivi, le nombre de décès par accidents cardiovasculaires fut de 10 dans le groupe régime/placebo, 26 dans les groupes tolbutamide et phenformine, 13 dans le groupe insuline à doses fixes et 12 dans le groupe insuline à doses variables.
Les conclusions de l’étude furent que les traitements par phenformine et tolbutamide étaient moins efficaces pour éviter les décès par accidents cardiovasculaires que les régimes seuls et les traitements insuliniques. À l’époque, on ne se hasardait pas à dire qu’un principe actif pouvait avoir des effets néfastes par rapport à un placebo. Il n’en reste pas moins que, compte tenu de sa méthodologie assez rustique, les résultats de cette étude furent rapidement controversés(7) : hétérogénéité des groupes, randomisation sans stratification en fonction des facteurs de risque, utilisation de doses fixes de phenformine et de tolbutamide pendant toute la durée de l’étude. À cette époque, la phenformine et le tolbutamide avaient déjà été jugés peu crédibles au sein de la classe des biguanides et des sulfonylurées. La phenformine (Insoral®) fut retirée quelques années après de la pharmacopée (en 1978 pour la France), quant au Dolipol® (tolbutamide), il était déjà en « fin de course ». Pour cette raison, les résultats de l’UGDP furent rapidement oubliés après avoir été largement commentés entre 1970 et 1972(7). Les sulfonylurées retrouvèrent leur popularité antérieure, surtout lorsque furent commercialisés les sulfamides de 2e génération.
Les sulfonylurées à la croisée du XXe et du XXIe siècle : un mécanisme d’action mieux appréhendé et une place relativement stable
Mécanisme d’action des sulfonylurées
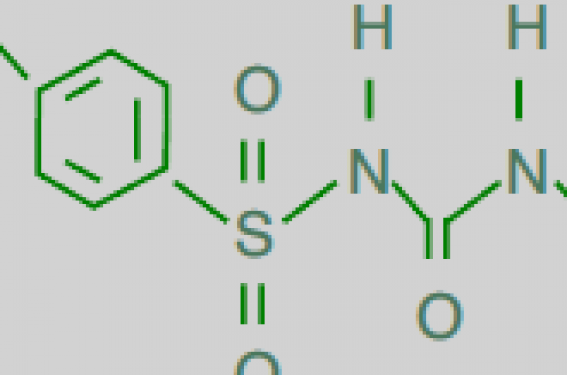
Les sulfonylurées tirent leur dénomination du fait qu’elles possèdent toutes un groupement moléculaire commun : le « groupe sulfonylurée » (figures 1 et 2). C’est ce groupement qui confère à ces substances la plus grande partie de leur effet hypoglycémiant. En dehors du gliclazide (figure 2), les sulfonylurées tirent également leur effet antidiabétique d’un deuxième groupement chimique : le groupe benzamidique (figure 1). Ces groupements benzamidiques sont différents d’un médicament à l’autre, ce qui explique que l’efficacité hypoglycémiante ne soit pas identique entre sulfonylurées.
Figure 1. Structure chimique des principales sulfonylurées possédant à la fois les groupements sulfonylurée et benzamidique.
Figure 2. Structure chimique du gliclazide, sulfonylurée ne possédant pas le groupement benzamidique.
Fixation des sulfonylurées sur le récepteur des cellules bêta
La sécrétion insulinique par la cellule ß est normalement régulée par la concentration du glucose extracellulaire qui pénètre à l’intérieur de la cellule ß après avoir été véhiculé par des transporteurs spécifiques : les GLUT2. Sans entrer dans les détails, le glucose active la glucokinase intracellulaire pour entraîner une augmentation du rapport ATP/ADP (figure 3)(8).
Cette augmentation s’accompagne d’une fermeture des canaux potassiques avec :
- diminution de l’efflux de K+ hors de la cellule ;
- dépolarisation de la membrane cellulaire ;
- augmentation de l’influx de Ca2+ à l’intérieur de la cellule par ouverture des canaux calciques ;
- in fine libération d’insuline.
La même cascade métabolique, à partir des canaux potassiques ATP-dépendants, peut être activée par la fixation des sulfonylurées sur un récepteur membranaire de la cellule ß : le SUR1 (figure 4a)(9). Ce récepteur est capable de reconnaître à la fois le groupement benzamidique et le groupement sulfonylurée. Le gliclazide, qui n’a pas de groupement benzamidique, a une affinité pour le récepteur plus faible que les autres sulfonylurées. Les résultats montrent que l’affinité des sulfonylurées pour le récepteur croît dans l’ordre suivant : gliclazide < glipizide < glimépiride < glibenclamide (glyburide). La différence d’affinité des sulfonylurées pour le récepteur SUR1 se traduit par une différence de capacité hypoglycémiante. Le glibenclamide reste à ce jour le ligand qui a la plus forte affinité pour le récepteur SUR1, suivi par le glimépiride puis le glipizide.
Figure 3. Mode d’action général des sulfonylurées au niveau des cellules bêta des îlots de Langerhans. La fixation de la sulfonylurée sur le récepteur membranaire est suivie d’une cascade métabolique qui conduit à la libération de l’insuline secrétée.
Figure 4. Fixation des sulfonylurées sur leurs récepteurs au niveau des cellules bêta pancréatiques (A) et des cellules musculaires vasculaires et cardiaques (B). b = groupement benzamidique ; s = groupement sulfonylurée. À noter qu’au niveau des récepteurs cardiovasculaires (B), la présence du groupement benzamidique (b) est indispensable, expliquant l’absence de fixation du gliclazide au niveau de ce type de récepteurs.
Fixation des sulfonylurées sur les récepteurs cardiaques et vasculaires
En dehors de leur fixation sur les cellules ß pancréatiques par l’intermédiaire du récepteur SUR1, les sulfonylurées peuvent se fixer sur d’autres tissus, en particulier sur les cellules musculaires cardiaques. Ce récepteur désigné sous le terme de SUR2A ne fixe que la partie benzamidique des sulfonylurées (figure 4b). Dans ces conditions, le gliclazide, sulfonylurée dépourvue du radical benzamidique, ne se fixerait pas sur les cellules cardiaques. Cette observation est importante car elle expliquerait pourquoi le gliclazide, à l’inverse des autres sulfonylurées comme le glibenclamide, ne perturberait pas l’adaptation du cardiomyocyte à l’ischémie, c’est-à-dire le phénomène de protection endogène contre l’ischémie myocardique encore appelé préconditionnement(10). Ce phénomène fait intervenir l’activation des canaux K+ ATP-dépendants. L’ischémie myocardique s’accompagne d’une diminution de la concentration intracellulaire en ATP, qui active à son tour les canaux K+ATP avec efflux de K+ hors de la cellule et diminution de l’influx Ca2+ à l’intérieur des cardiomyocytes et des cellules musculaires des parois artérielles. Ces phénomènes contribuent à diminuer le tonus vasculaire et à accroître le débit sanguin. Les sulfonylurées, en fermant les canaux potassiques, entraveraient ce système d’adaptation et pourraient contribuer à aggraver les phénomènes ischémiques chez un sujet venant de présenter une nécrose myocardique. Les sulfonylurées comme le glibenclamide, en se fixant sur les récepteurs SUR2A par l’intermédiaire de leur radical benzamidique, seraient les plus néfastes. Le gliclazide n’ayant pas ce radical, serait dépourvu de ce type d’effet et n’entraverait pas les phénomènes d’adaptation à l’ischémie.
Ces considérations théoriques sont-elles confirmées par les études cliniques ? À ce jour, aucune étude ne permet d’étayer l’hypothèse que certaines sulfonylurées auraient un rôle protecteur ou un rôle aggravant sur l’évolution des nécroses myocardiques(11). D’un point de vue plus général, à partir des résultats de l’UKPDS(6), des études ADOPT(12) et ADVANCE(13), nul ne peut affirmer que les sulfonylurées modifient dans un sens favorable ou défavorable l’incidence des décès par accidents cardiovasculaires. L’étude ADVANCE(13) dans laquelle le groupe intensif a été soumis à un traitement par gliclazide aurait pu fournir quelqueséléments de réponse, mais en dehors d’une diminution modeste des complications rénales, qui répondent à un mécanisme différent de celui des complications macrovasculaires, aucune différence n’a été notée en termes d’incidence des décès d’origine cardiovasculaire entre le groupe intensif (gliclazide) et le groupe conventionnel. Dans les suites d’infarctus du myocarde, la meilleure protection cardiovasculaire, établie à partir des études DIGAMI 1(14) et DIGAMI 2(15), semble être la correction des perturbations glycémiques à condition d’éviter les hypoglycémies quel que soit le moyen utilisé pour obtenir l’équilibre glycémique. Toutefois une préférence devrait être donnée aux traitements insuliniques en raison de leurs effets pléiotropes propres : anti-inflammatoires, antithrombotiques et anti-stress oxydant(16).
Place des sulfonylurées dans l’organigramme thérapeutique du diabète de type 2
Aujourd’hui, cette place paraît relativement stabilisée bien que les différentes organisations n’aient pas une vue identique sur la question. La seule certitude est que les sulfonylurées, qui apparaissaient en première ligne dans les années 1970-80, en balance avec les biguanides, ont perdu cette place. Désormais, elles apparaissent comme des traitements de 2e ou 3e intention, la metformine étant devenue le traitement de choix en 1re intention(5).
Le consensus ADA/EASD place les sulfonylurées en 2e intention et sur la même ligne de choix que les thiazolidinediones (TZD), les inhibiteurs de la DPP4, les agonistes des récepteurs du GLP1 et même l’insuline(5). À notre avis, ce choix devrait être mieux précisé car il est déjà un peu illogique de mettre sur le même plan en 2e intention des préparations orales et injectables. Notre position personnelle est la suivante(17). En cas d’échec de la metformine et, sauf cas particulier (sujet très déséquilibré, affection intercurrente nécessitant une insulinothérapie), la priorité devrait être donnée à un antidiabétique oral. Le choix en 2e intention est relativement simple : inhibiteurs de la DPP4 ou sulfonylurées, c’est-à-dire insulinosécrétagogues glucodépendants versus insulinosécrétagogues non glucodépendants. Dès lors, le choix peut être modulé de la manière suivante (figure 5)(17). Toutefois, ce choix va être élargi grâce à la venue sur le marché des inhibiteurs du SGLT2.
Figure 5. Choix thérapeutique de 2e intention (inhibiteur de la DPP4 ou sulfonylurée) en fonction du niveau de l’HbA1c(17).
Chez des sujets ayant une HbA1c < 7,5-8 %, c’est l’hyperglycémie postprandiale qui prédomine par rapport à l’hyper glycémie basale. Dans ces conditions, les inhibiteurs de la DPP4, qui agissent plutôt sur les glycémies postprandiales, paraissent davantage justifiés que les sulfonylurées dont l’effet est surtout de type basal.
Dans le cas contraire, HbA1c > 7,5-8 %, il est préférable de préconiser l’utilisation des sulfonylurées.
La sécurité du traitement justifie également ce choix. Essayer de ramener l’HbA1c d’un diabétique en dessous de 6,5 % quand il garde une HbA1c entre 6,5 % et 7,5 % ne peut se faire qu’avec des médicaments dénués de tout risque d’hypoglycémie : aujourd’hui les inhibiteurs de la DPP4, auxquels il faudra rajouter les inhibiteurs SGLT2.
En revanche, quand l’HbA1c est < 7,5-8 %, les sulfonylurées sont plutôt contre-indiquées en raison de leur mode d’action : stimulation de l’insulinosécrétion endogène sur un mode non glucodépendant. À cet égard, les recommandations de la HAS (Haute Autorité de santé) nous paraissent fortement critiquables(18) car elles privilégient sans grand discernement physiopathologique les sulfonylurées par rapport aux inhibiteurs de la DPP4. Une analyse un peu plus subtile des indications respectives des deux classes thérapeutiques aurait été souhaitable, si ce n’est indispensable.
Conclusion
Au terme de cet article, il apparaît que 70 ans après leur découverte, les sulfonylurées restent une classe thérapeutique qui garde toute sa place parmi les médications antidiabétiques.
Quelques années après leur découverte et leur mise sur le marché, certains avaient pensé que les sulfonylurées auraient pu avoir, en plus de leur effet insulinosécrétoire, un effet bêta « cytotrophe ». Faire repousser les cellules ß avec un traitement oral est un vieux rêve récurrent. Évoqué à l’époque pour les sulfonylurées, mais rapidement réfuté par l’expérience, ce vieux rêve resurgit périodiquement chaque fois qu’apparaît un nouvel antidiabétique. À ce jour, ni les glitazones ni les médications basées sur l’effet incrétine n’ont jamais montré, en dépit de travaux expérimentaux, un quelconque effet protecteur ou régénérateur sur les cellules ß des îlots de Langerhans.
Laissons donc les sulfonylurées exercer leurs effets propres sans tenter de leur trouver d’autres propriétés pléiotropes, plus ou moins merveilleuses, voire miraculeuses, comme certains ont pu le prétendre ou l’espérer pour certaines variétés de sulfonylurées.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :